1. Pengertian
Laju Reaksi
Laju menyatakan seberapa cepat atau seberapa lambat
suatu proses berlangsung. Laju juga menyatakan besarnya perubahan yang terjadi
dalam satu satua waktu. Satuan waktu dapat berupa detik, menit, jam, hari atau
tahun.
Reaksi kimia adalah proses perubahan zat pereaksi menjadi produk. Seiring dengan bertambahnya waktu reaksi, maka jumlah zat peraksi semakin sedikit, sedangkan produk semakin banyak. Laju reaksi dinyatakan sebagai laju berkurangnya pereaksi atau laju terbentuknya produk.
Reaksi kimia adalah proses perubahan zat pereaksi menjadi produk. Seiring dengan bertambahnya waktu reaksi, maka jumlah zat peraksi semakin sedikit, sedangkan produk semakin banyak. Laju reaksi dinyatakan sebagai laju berkurangnya pereaksi atau laju terbentuknya produk.
2. Ungkapan Laju Reaksi untuk Sistem Homogen
Untuk sistem homogen, laju reaksi umum dinyatakan
sebagai laju penguragan konsentrasi molar pereaksi atau laju pertambahan
konsentrasi molar produk untuk satu satuan waktu, sebagai berikut:
Jika diketahui satuan dari konsentrasi molar adalah
mol/L. Maka satuan dari laju reaksi adalah mol/L.det atau M/det.
3. Laju Rerata
dan Laju Sesaat
a. Laju rerata
Laju rerata adalah rerata laju untuk selang waktu
tertentu. Perbedaan antara laju rerata dengan laju sesaat dapat diandaikan
dengan laju kendaraan. Misalnya suatu kendaraan menempuh jarak 300 km dalam 5
jam. Laju rerata kendaraan itu adalah 300 km/5 jam = 60 km/jam. Tentu saja laju
kendaraan tidak selalu 60 km/jam. Laju sesaat ditunjukkan oleh speedometer
kendaraan.
b. Laju Sesaat
Laju sesaat adalah laju pada saat tertentu. Sebagai
telah kita lihat sebelumnya, laju reaksi berubah dari waktu ke waktu. Pada umumnya,
laju reaksi makin kecil seiring dengan bertambahnya waktu reaksi. oleh karena
itu, plot konsentrasi terhadap waktu berbentuk garis lengkung, seperti gambar
di bawah ini. Laju sesaat pada waktu t dapat ditentukan dari kemiringan (gradien)
tangen pada saat t tersebut, sebagai berikut.
- Lukis garis singgung pada saat t
- Lukis segitiga untuk menentukan kemiringan
- laju sesaat = kemiringan tangen
FAKTOR-FAKTOR YANG MEMPENGARUHI LAJU REAKSI
1. Konsentrasi Pereaksi
Konsentrasi memiliki peranan yang sangat penting dalam
laju reaksi, sebab semakin besarkonsentrasi pereaksi, maka tumbukan yang
terjadi semakin banyak, sehingga menyebabkan laju reaksi semakin cepat. Begitu
juga, apabila semakin kecil konsentrasi pereaksi, maka semakin kecil tumbukan
yang terjadi antar partikel, sehingga laju reaksi pun semakin kecil.
2. Suhu
Suhu juga turut berperan dalam mempengaruhi laju
reaksi. Apabila suhu pada suatu rekasi yang berlangusng dinaikkan, maka
menyebabkan partikel semakin aktif bergerak, sehingga tumbukan yang terjadi
semakin sering, menyebabkan laju reaksi semakin besar. Sebaliknya, apabila suhu
diturunkan, maka partikel semakin tak aktif, sehingga laju reaksi semakin
kecil.
3. Tekanan
Banyak reaksi yang melibatkan pereaksi dalam wujud
gas. Kelajuan dari pereaksi seperti itu juga dipengaruhi tekanan. Penambahan
tekanan dengan memperkecil volume akan memperbesar konsentrasi, dengan demikian
dapat memperbesar laju reaksi.
4. Katalis
Katalis adalah suatu zat yang mempercepat laju reaksi
kimia pada suhu tertentu, tanpa mengalami perubahan atau terpakai oleh reaksi
itu sendiri. Suatu katalis berperan dalam reaksi tapi bukan sebagai pereaksi
ataupun produk. Katalis memungkinkan reaksi berlangsung lebih cepat atau
memungkinkan reaksi pada suhu lebih rendah akibat perubahan yang dipicunya
terhadap pereaksi. Katalis menyediakan suatu jalur pilihan dengan energi
aktivasi yang lebih rendah. Katalis mengurangi energi yang dibutuhkan untuk
berlangsungnya reaksi.
5. Luas Permukaan Sentuh
Luas permukaan sentuh memiliki peranan yang sangat
penting dalam laju reaksi, sebab semakin besar luas permukaan bidang sentuh
antar partikel, maka tumbukan yang terjadi semakin banyak, sehingga menyebabkan
laju reaksi semakin cepat. Begitu juga, apabila semakin kecil luas permukaan bidang
sentuh, maka semakin kecil tumbukan yang terjadi antar partikel, sehingga laju
reaksi pun semakin kecil. Karakteristik kepingan yang direaksikan juga turut
berpengaruh, yaitu semakin halus kepingan itu, maka semakin cepat waktu yang
dibutuhkan untuk bereaksi; sedangkan semakin kasar kepingan itu, maka semakin
lama waktu yang dibutuhkan untuk bereaksi.

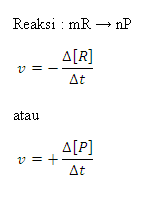


Tidak ada komentar:
Posting Komentar